近日,上海理工大学东方泛血管器械创新学院叶士伟博士后作为第一作者以“蛋白激酶C激动剂可改善生物生成缺陷型囊性纤维化跨膜传导调节因子的功能”为题,在《分子疗法》(Molecular Therap)上发表研究成果。上海理工大学是该论文的第一完成单位,论文的通讯作者是蔡时青研究员(上海交通大学)和沈雳教授(上海理工大学、复旦大学)。该研究发现一类新型小分子化合物——蛋白激酶C(PKC)激动剂,能够通过一种全新机制提升突变囊性纤维化跨膜传导调节因子(CFTR)的生物生成(biogenesis)效率,并与现有药物产生叠加效应,为囊性纤维化患者提供了新的治疗策略。
囊性纤维化是一种常染色体隐性遗传病,由位于7号染色体上的CFTR基因突变所致。CFTR基因编码的CFTR蛋白是细胞膜上负责氯离子转运的离子通道,其最常见的F508del突变(即CFTR蛋白第508位苯丙氨酸缺失)会导致CFTR通道蛋白发生错误折叠,并影响其正常运输,最终使其无法在细胞膜上形成功能性的氯离子通道。囊性纤维化可累及多器官系统,包括呼吸道、消化道及生殖系统等。以呼吸系统为例,患者气道因黏液过度黏稠而致阻塞,引发呼吸困难;同时,黏液环境易致细菌定植与感染,进而造成广泛肺纤维化,最终可进展为呼吸衰竭甚至死亡。当前临床治疗以CFTR调节剂疗法为主,通常采用校正剂(如Lumacaftor、Tezacaftor、Elexacaftor)与增效剂(如Ivacaftor)联合应用。然而,大部分患者的功能恢复仍不彻底,且部分突变类型对现有疗法不敏感。
研究团队发现,两种PKC激动剂IDB和DOPPA能从源头上增强CFTR蛋白的合成效率。与现有药物主要通过辅助蛋白折叠或运输不同,PKC激动剂通过激活PKCε信号通路,在蛋白翻译阶段对新生CFTR肽链进行磷酸化修饰,阻止其因折叠缺陷而被提前降解。这种稳定的翻译过程确保了核糖体在其 mRNA上的持续占据,以空间位阻效应阻断核酸内切酶切割。因此,这一机制不仅能提高CFTR mRNA的稳定性,还可持续提升功能性CFTR蛋白的表达量。如果把现有校正剂比作“修理工”,那么PKC激动剂更像是“生产线提速员”。它们从源头上增加了可被校正的蛋白数量,因此与现有药物联用能够产生的叠加效果。
总的来说,该研究不仅揭示了一条此前未被重视的CFTR生物生成调控通路,也为开发针对多种CFTR突变类型的“放大器”类药物提供了理论依据。目前,研究团队正进一步探究其他激酶对CFTR生物生成的影响,同时优化PKC激动剂的结构和功能,并探究其在长QT间期综合征、先天性耳聋及发作性共济失调等离子通道病中的应用潜力。
该研究工作由国家自然科学基金委员会和科学技术部相关项目资助。
 论文截图
论文截图
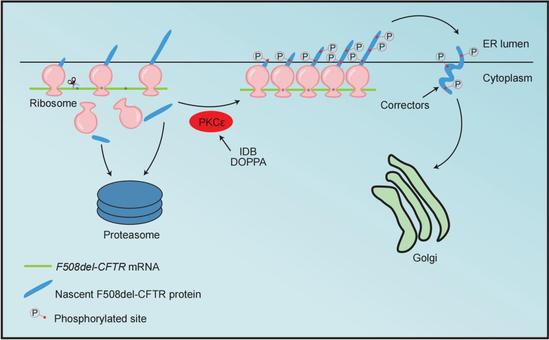 论文原理图
论文原理图










